Inactivés mais pas bouchés !
À Brest, des chimistes agissent sur le développement de métastases en bloquant des canaux ioniques, sans les boucher.
La première solution qui vient à l’esprit quand on veut bloquer un canal (ou un tuyau) est de le boucher. Mais la nature est parfois plus complexe. Tel est le cas qui occupe une équipe de chimistes de l’UBO(1), à Brest(2) depuis plusieurs années.
Les canaux en question se trouvent ancrés à l’intérieur des membranes de nombreuses cellules. Il s’agit de canaux ioniques qui, comme leur nom l’indique, contrôlent le passage des ions (chargés positivement ou négativement) créant, ou non, des différences de milieux (acidité, conductivité...) entre l’intérieur et l’extérieur de la cellule. Or, certains de ces canaux jouent un rôle essentiel dans le développement des métastases osseuses ou pulmonaires de certains cancers très invasifs (sein, prostate). « Le mécanisme d’action d’Ohmline, la molécule inhibitrice que nous avons synthétisée, est original car elle s’insère à l’intérieur de la membrane et non directement dans le canal, explique Paul-Alain Jaffrès, responsable de l’équipe. En pénétrant dans la membrane, elle modifie ses propriétés biophysiques et donc la stabilité et l’activité des canaux ioniques alentour. Et le résultat est net : cela contribue à bloquer le développement des métastases. »
Cette originalité a fait l’objet d’une publication en 2013(3) et, depuis, Paul-Alain Jaffrès et ses collègues en ont appris un peu plus : la molécule est sélective ! Il existe en effet quatre canaux ioniques (qui laissent passer des ions potassium) qui se ressemblent (SK1, 2, 3 et 4) et Ohmline n’agit que sur SK3 et un peu sur SK1. Pourquoi ? Les chercheurs ne le savent pas encore.
Le jeu des différences
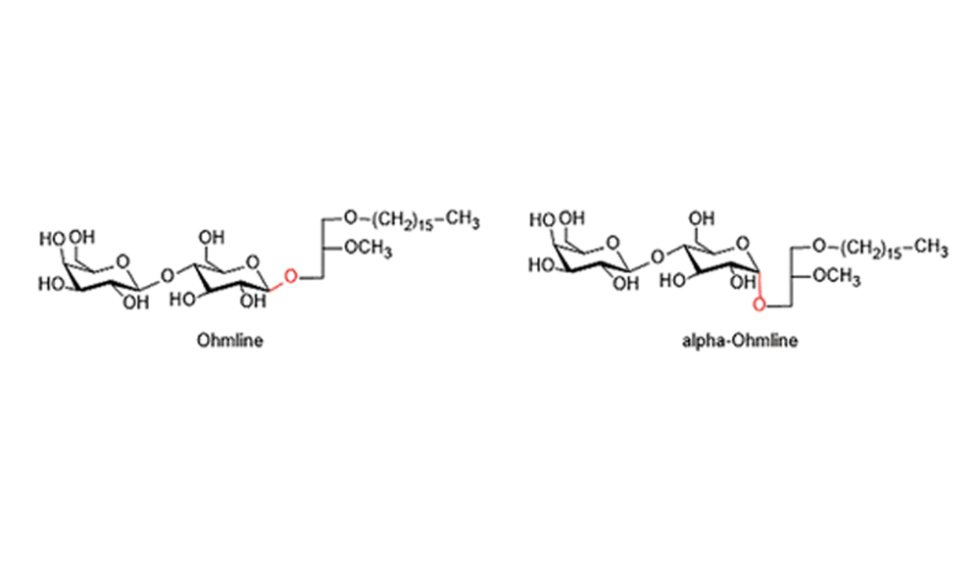
Pour comprendre plus finement le mécanisme d’action d’une molécule, la technique des chimistes consiste à fabriquer des analogues : ils partent de leur molécule d’origine (Ohmline) et en créent de nouvelles avec de petites différences : remplacement d’un atome par un autre ; changement de configuration d’un groupe d’atomes (voir schéma)... et regardent quelles incidences ont ces modifications. Pour l’instant, ils ont identifié un changement qui inactive complètement la molécule et un autre (trouvé par hasard) qui stimule l’activité des canaux ioniques. « Activer les canaux n’est évidemment pas ce que nous cherchons pour stopper le développement des métastases, mais ce résultat est fondamentalement intéressant et se révélera peut-être utile dans un autre contexte, pour le traitement d’une autre pathologie. »
L’avis précieux des industriels
Ce mécanisme original et ces premiers résultats ont déjà permis aux chercheurs d’arriver en final du concours Matwin(4) en 2015, dont le but est de mettre en contact les responsables scientifiques des grands groupes industriels pharmaceutiques avec des chercheurs des laboratoires académiques. « Nous avons apprécié le fait d’avoir un retour sur la façon dont était perçue notre technique, explique Paul-Alain Jaffrès. Notre molécule a séduit par sa non-toxicité, par exemple. Mais elle n’agit que sur les métastases et pas sur la tumeur primaire... » Les chimistes ouvrent des voies. Après, le chemin jusqu’au médicament est encore long !
(1) Université de Bretagne Occidentale, laboratoire Cemca, UBO/ UMR CNRS.
(2) Dans le cadre d’un projet mené en collaboration au sein du Cancéropole Grand Ouest avec l’équipe d’électrophysiologistes du Pr. C. Vandier de l’université de Tours (Inserm UMR 1069) et financé par la Ligue contre le cancer.
(3) Lire Métastases : une voie de blocage dans Sciences Ouest n° 313- octobre 2013.
(4) Maturation & accelerating translation with industrials.
(5) Berthe, W. ; Sevrain, C.M. ; Chantôme, A. ; Bouchet, A.M. ; Gueguinou,
M. ; Fourbon,Y. ; Potier-Cartereau, M. ; Haelters, J.P. ; Couthon-Gourvès, H. ; Vandier, C. ; Jaffrès, P.A. ChemMedChem, 2016, 11, 1531-1539.
Paul-Alain Jaffrès
tél. 02 98 01 61 53
Paul-Alain.Jaffres@univ-brest.fr
TOUT LE DOSSIER
du magazine Sciences Ouest






